Unsere mRNA-Plattformen – Impfstofftechnologie revolutionieren
Unsere mRNA-Plattformen wurden so konzipiert, dass sie das Immunsystem über verschiedene Wege aktivieren bzw. modulieren können. Hierbei bietet jeder Ansatz eine bestimmte Strategie, um Krebs zu bekämpfen oder vor Infektionskrankheiten zu schützen.
FixVac –indikationsspezifische off-the-shelf Krebsimpfstoffe
Auch wenn die jeweiligen Tumore von Patientinnen und Patienten einzigartig sind, können sie bestimmte Marker, sogenannte Antigene, gemeinsam haben. Diese Marker kommen häufig in bestimmten Krebsarten vor und werden oft in vielen Patientinnen und Patienten mit der gleichen Krebsart exprimiert – kommen aber nicht in gesunden Körperzellen vor. Da Krebszellen Mechanismen entwickelt haben, um der Erkennung durch das Immunsystem zu entgehen, besteht eine große Herausforderung bei der erfolgreichen Behandlung von Krebs darin, dass das Immunsystem die Krebszellen nicht als bösartige Zellen erkennt und somit keine Immunreaktion auslöst, um diesen Feind anzugreifen und zu besiegen. Indem wir dem Immunsystem die richtigen Antigene für jede Krebsindikation präsentieren, können wir Immunzellen aktivieren, die spezifisch krebstypspezifische Antigene erkennen und sie gegen die Krebszellen richten. Diese Idee ist die Grundlage für unsere FixVac mRNA-Krebsimpfstoff-Plattform.
Architektur unserer FixVac Plattform
Unsere FixVac-Plattformkandidaten bestehen aus einer festen Impfstoff-Kombination (fixed vaccine combination) von mRNA-kodierten, nicht-mutierten Tumorantigenen, die in bestimmten Krebsarten gehäuft vorkommen. Die mRNA wird mit unserer unternehmenseigenen RNA-Lipoplex-Formulierung verabreicht, die die Stabilität und Translation der enthaltenen mRNA im Körper verbessert und diese speziell zu Antigen-präsentierenden dendritischen Zellen (DCs) transportiert – den Hochleistungstrainern des Immunsystems. Indem sie die Präsentation dieser spezifischen Tumorantigene durch DCs für das Immunsystem verbessern, zielen unsere FixVac-Kandidaten darauf ab, eine starke und präzise angeborene und adaptive Immunantwort gegen Krebszellen auszulösen, die eines oder mehrere der jeweiligen Tumorantigene exprimieren. Dieser Ansatz bietet die Möglichkeit, auch Tumore mit einer geringen Mutationslast effektiv zu behandeln, was z.B. bei der Hälfte aller Patientinnen und Patienten mit metastasiertem Melanomen der Fall ist.

Wir nutzen optimierte Uridin-basierte mRNA (uRNA) für unsere FixVac-Kandidaten, um ihren immunstimulierenden Effekt zu verbessern und so die Wirksamkeit des Impfstoffs zu verstärken – eine der größten Herausforderungen, die derzeit in Studien mit Tumorantigen-basierten Krebsimpfstoffen beobachtet werden.
Unser Ziel ist es, mit diesem neuartigen, mRNA-basierten Krebsimpfstoff-Ansatz eine Behandlung bereitzustellen, die einerseits als off-the-shelf-Therapie hergestellt werden kann und andererseits hochspezifisch für die jeweilige Tumorart ist, – insbesondere für Patientinnen und Patienten mit fortgeschrittenen, schwer behandelbaren Krebserkrankungen.
Auf einen Blick: Unsere FixVac-Plattform
Konzept: Feste Kombination mRNA-kodierter Tumor-Antigene, die in bestimmten Krebsarten gehäuft vorkommen. Hiermit soll eine starke und präzise Immunantwort gegen Krebszellen ausgelöst werden, die das jeweilige Antigen exprimieren
mRNA-Format: Optimierte Uridin-basierte mRNA (uRNA) für verbesserte Impfstoffwirksamkeit
Therapiebereiche: Solide Tumore, einschließlich Melanome, Prostatakrebs, HPV16-positive Plattenepithelkarzinome des Kopfs und Halses, Eierstockkarzinom und nicht-kleinzelliges Lungenkarzinom
iNeST – individualisierte mRNA-Krebsimpfstoffe
Wir sind weltweit einer der führenden Pioniere bei der Entwicklung vollständig individualisierter Immuntherapien, die darauf abzielen, den individuellen Tumor eines Patienten bzw. einer Patientin zu adressieren. Mit unserer Plattform zur individualisierten Neoantigen-spezifischen Immuntherapie (Individualized Neoantigen Specific Immunotherapy, iNeST) haben wir einen neuartigen, bedarfsgerechten Herstellungsprozess für mRNA-Impfstoffe entwickelt, die auf sogenannte Tumor-Neoantigene abzielen – Mutationen, die einzigartig für den spezifischen Tumor des jeweiligen Patienten sind.
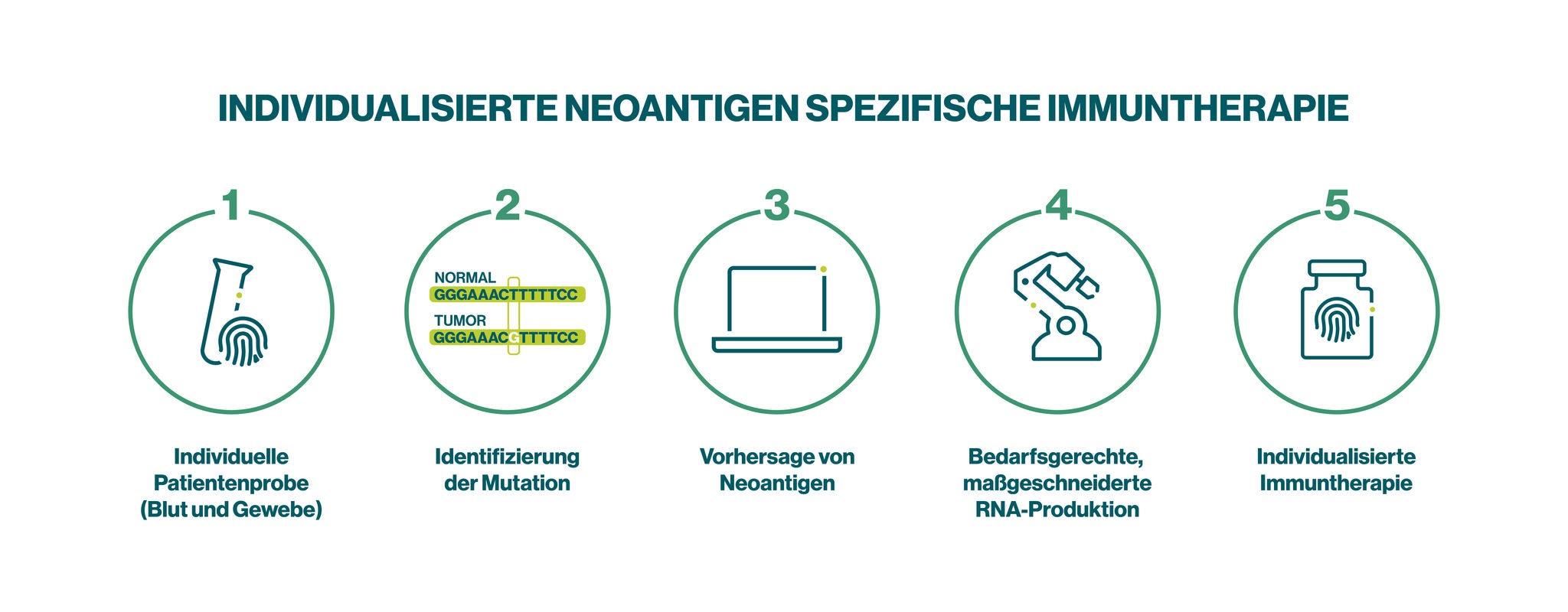
Unsere iNeST-Kandidaten enthalten mRNA, die für eine individuell ausgewählte Anzahl von patientenspezifischen Tumor-Neoantigenen kodiert. Hiermit soll eine starke und präzise Immunantwort gegen den einzigartigen Tumor des jeweiligen Patienten ausgelöst werden.

Wir nutzen optimierte Uridin-basierte mRNA (uRNA) für unsere iNeST-Kandidaten, um ihren immunstimulierenden Effekt zu verbessern und so die Wirksamkeit des Impfstoffs zu verstärken – eine der größten Herausforderungen, die derzeit in Studien mit Tumorantigen-basierten Impfstoffen beobachtet werden.
Weitere Informationen zur iNeST-Produktion und dem Behandlungsprozess finden Sie in folgendem Fact Sheet.
Auf einen Blick: Unsere iNeST-Plattform
Konzept: Individualisierter mRNA-Krebsimpfstoff, der für eine individuell ausgewählte Anzahl von patientenspezifischen Neoantigenen kodiert, um eine starke und präzise Immunantwort gegen den individuellen Tumor des jeweiligen Patienten bzw. der jeweiligen Patientin auszulösen
mRNA Format: Optimierte Uridin-basierte mRNA (uRNA) für verbesserte Impfstoffwirksamkeit
Therapiebereiche: Solide Tumore, einschließlich Melanomen und Darmkrebs
Impfstoff gegen Infektionskrankheiten – unsere revolutionäre Technologieplattform für prophylaktische Impfstoffe
Unsere mRNA-Impfstoffe wurden entwickelt, um das Immunsystem für eine effektive Erkennung und Bekämpfung spezifischer Pathogene zu trainieren. Sie kodieren für den Bauplan eines nicht-infektiösen Pathogenfragments, dem sogenannten Immunogen, und transportieren diesen zu Antigen-präsentierenden Zellen (APCs) im Körper. Dort wird das Immunogen hergestellt und an die Immunzellen des Körpers präsentiert.
Mit diesem Ansatz lernen die Immunzellen, wie man den Krankheitserreger erkennt und bekämpft und können so im Fall einer tatsächlichen Infektion schnell reagieren und das Pathogen eliminieren. Diese schnelle Reaktion reduziert signifikant das Risiko für eine Pathogen-induzierte Erkrankung sowie einer Übertragung des Krankheitserregers auf andere Menschen.

Wir nutzen nukleosidmodifizierte mRNA (modRNA) für unsere mRNA-Impfstoffkandidaten, die natürlich vorkommende, modifizierte Bausteine für eine verbesserte Stabilität und reduzierte Immunogenität enthalten, um so ungewollte Immunreaktionen zu minimieren und die Dauer der Proteinproduktion zu verlängern – zwei der größten Herausforderungen bei der Entwicklung sicherer und wirksamer mRNA-Impfstoffe.
Unsere mRNA-Impfstoffplattform hat die Entwicklung des ersten kommerziell erhältlichen COVID-19-Impfstoffs ermöglicht – ein klarer Beweis für die Bedeutung und Wirksamkeit unserer Plattformtechnologie.
Hier finden Sie weitere Informationen über unseren COVID-19-Impfstoff und Projekt Lightspeed.
Erfahren Sie mehr über die Infektionskrankheiten, die wir adressieren.
Auf einen Blick: Unsere mRNA-Impfstoff-Plattform
Konzept: mRNA-Impfstoffe kodieren für ein oder mehrere nicht-infektiöse Pathogenfragmente, um das Immunsystem für die Erkennung und Bekämpfung des jeweiligen Krankheitserregers im Fall einer tatsächlichen Infektion zu trainieren
mRNA-Format: nukleosidmodifizierte mRNA (modRNA) zur Minimierung ungewollter Immunreaktionen und verlängerter Dauer der Proteinproduktion
Therapiebereiche: Infektionskrankheiten, einschließlich COVID-19, saisonale Grippe, Malaria, HIV und Tuberkulose
RiboMab – Ein neuartiger Ansatz für Antikörpertherapien
Unsere RiboMab (mRNA, die für bispezifische monoklonale Antikörper (mAb)-kodierende mRNA)-Kandidaten stellen die nächste Generation Antikörper-basierten Therapien gegen Krebs und Infektionskrankheiten dar. Sie sollen die derzeitigen Herausforderungen klassischer rekombinanter Protein-Antikörper überwinden, wie beispielsweise den langwierigen Protein-Herstellungsprozess. Mit diesem revolutionären neuartigen Ansatz können wir dem menschlichen Körper direkt einen mRNA-kodierten Bauplan für therapeutische Antikörper, den sogenannten RiboMabs, zur Verfügung stellen. Durch diesen Ansatz sind insbesondere kleinere Antikörperderivate wesentlich länger im Körper verfügbar. Wir glauben, dass dadurch, im Gegensatz zur Therapie mit rekombinanten Protein-Antikörpern die Anzahl der benötigten Injektionen verringert und der Einsatz von Infusionspumpen vermieden werden kann. Darüber hinaus soll durch die körpereigene Produktion eine mögliche unerwünschte Immunreaktion gegen den therapeutischen Antikörper selbst deutlich minimiert werden – ein Problem, das beim rekombinanten Ansatz häufig auftritt. Die erfolgreiche Verabreichung unserer RiboMabs-Kandidaten in Form eines speziell formulierten mRNA-Codes macht unseren therapeutischen Antikörper-Ansatz einfacher, schneller und kostengünstiger im Vergleich zu herkömmlichen Antikörper-Therapien. Unser RiboMabs-Ansatz ermöglicht zudem die Untersuchung möglicher neuer Zielstrukturen, beschleunigt die Entwicklung und klinische Evaluierung neuer Produktkandidaten und eröffnet möglicherweise auch den Einsatz in neuen Indikationen.

Wir nutzen nukleosidmodifizierte mRNA (modRNA) für unsere RiboMabs-Kandidaten, die natürlich vorkommende, modifizierte Bausteine für eine verbesserte Stabilität und reduzierte Immunogenität enthalten, um so ungewollte Immunreaktionen zu minimieren und die Dauer der Proteinproduktion zu verlängern – zwei der größten Herausforderungen bei der Entwicklung sicherer und wirksamer mRNA-Impfstoffe.
Auf einen Blick: Unsere RiboMab-Plattform
Konzept: mRNA-kodierte Antikörper gegen Krebs und Infektionskrankheiten, die als Alternative zu rekombinanten Antikörpern dienen und direkt im Körper der Patientin bzw. des Patienten produziert werden
mRNA-Format: nukleosidmodifizierte mRNA (modRNA) zur Minimierung ungewollter Immunreaktionen und verlängerter Dauer der Proteinproduktion
Therapiebereiche: Solide Tumore, einschließlich Magenkrebs und Pankreaskarzinom, sowie Infektionskrankheiten, einschließlich HIV
Mehr entdecken

Pipeline

Publikationen
